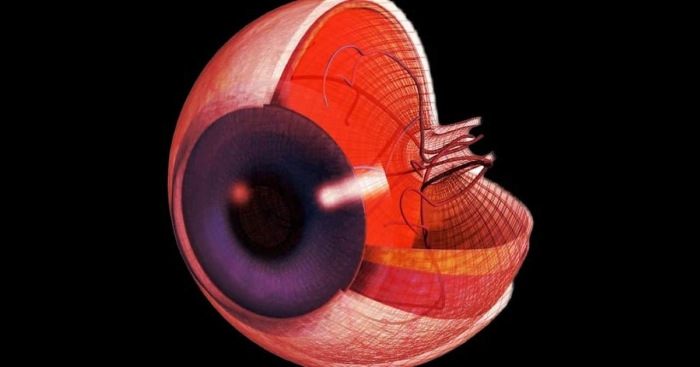
Исследования болезней глаз человека и функционирования нейронов затруднены тем, что эти органы стремительно деградируют опосля погибели. Не считая того, глаза звериных различаются от наших. Чтоб поправить ситуацию, интернациональная группа исследователей разработала новейший способ “возврата к жизни” сетчатки глаза, взятой у доноров через 5 часов опосля их погибели. Это техническое достижение дозволит провести новейшие исследования функционирования людского глаза и нервной системы, также продлить срок жизни пересаживаемых органов. Этот фуррор также открывает новейшие перспективы для исцеления нейродегенеративных болезней, включая возрастную макулярную дегенерацию.
Погибель определяется как необратимое прекращение кровообращения, дыхания либо работы мозга. Почти все периферические органы человека могут быть пересажены от погибших доноров с внедрением протоколов для оптимизации жизнеспособности. Но ткани центральной нервной системы и некие связанные с ней органы, такие как глаза, стремительно теряют жизнеспособность опосля прекращения кровообращения, что затрудняет их трансплантационный потенциал. Это происходит поэтому, что млрд нейронов в центральной нервной системе передают сенсорную информацию в виде электронных сигналов; в глазу спец нейроны, именуемые фоторецепторами, обнаруживают свет. Эти клеточки стремительно гибнут опосля остановки сердца. Но временной ход и механизмы, вызывающие смерть нейронов, также возможность реактивации остаются плохо изученными.
Чтоб лучше осознать, как нервные клеточки реагируют на недочет кислорода, вызванный прекращением общего кровообращения, команда американских и швейцарских исследователей употребляла сетчатку глаза в качестве модели центральной нервной системы. Они измерили активность мышиных и человечьих клеток сетчатки скоро опосля их погибели и разработали новейшие способы, дозволяющие возвратить их к жизни. Их работа размещена в журнальчике Nature.
Восстановление связи меж клеточками опосля погибели
Для заслуги собственной цели доцент кафедры исследовательских работ Скриппса Энн Ханнекен смогла предоставить наиболее 40 глаз от доноров органов в течение 20 минут опосля погибели. Франс Винберг из Глазного центра Морана разработал особое транспортное устройство для восстановления кислорода и остальных питательных веществ в очах донора, также устройство для стимуляции сетчатки и измерения электронной активности ее клеток. Потому команда работала в два шага.
Во-1-х, исследователи показали резвое понижение сигнализации нейронов и обусловили условия, нужные для возможной реанимации клеток глаза in vivo у мышей опосля погибели и в сетчатке человека. На втором шаге они измерили светоиндуцированные реакции в фоторецепторах макулы человека из донорских глаз через 5 часов опосля погибели. Потом они смогли найти модифицируемые причины, приводящие к обратимой и необратимой потере передачи световых сигналов опосля погибели.
Хотя 1-ые опыты возродили фоторецепторы, оказалось, что клеточки утратили способность разговаривать с иными клеточками сетчатки. Команда обусловила кислородное голодание как критичный фактор, приводящий к потере связи.
Фатима Аббас, сотрудник Глазного центра Морана и ведущий создатель исследования, объясняет в собственном заявлении: “Мы смогли пробудить фоторецепторные клеточки в макуле человека, которая является частью сетчатки, отвечающей за центральное зрение и способность созидать маленькие детали и цвета. В очах, приобретенных через 5 часов опосля погибели донора органов, эти клеточки реагировали на броский свет, цветной свет и даже весьма слабенькие вспышки света”.
Используя собственный инноваторский подход к поддержанию кислорода в клеточках в течение наиболее долгих периодов времени, что наращивает время выживания сетчатки и клеток нейронов, команда смогла вернуть специфичный электронный сигнал, наблюдаемый в {живых} очах, “b-волна”. Средством b-волн осуществляется связь меж всеми слоями клеток макулы, которые разрешают нам созидать. Это 1-ая посмертная запись b-волны из центра сетчатки глаза человека. Но это временное восстановление активности клеток сетчатки не значит, что донорские глазные яблоки могли “созидать”. Для оживления всего процесса зрения нужны наиболее высочайшие зрительные центры в мозге.
Франс Винберг гласит: “Мы смогли вынудить клеточки сетчатки разговаривать, как они это делают в живом глазу, опосредуя человеческое зрение. Прошлые исследования вернули весьма ограниченную электронную активность в очах доноров органов, но это никогда не было достигнуто в макуле, и никогда в той степени, которую мы на данный момент показали”.
В связи с этими плодами некие специалисты ставят под колебание необратимый нрав погибели в центральной нервной системе. Вправду, хотя некие органы людского тела можно сохранить для трансплантации, центральная нервная система перестает работать очень стремительно, чтоб ее можно было “вернуть” для пересадки. Но не все составляющие нашей нервной системы погибают с схожей скоростью, а время от времени механизмы “выживания” инсталлируются на некое время, что делает понятие погибели наиболее сложным. В этом контексте подвиги, описанные в статье, дадут наиболее четкую картину (без каламбура) и укажут на новейшие способности для мед достижений.
Исследование нейродегенеративных болезней
Таковым образом, продемонстрированный командой процесс быть может применен для исследования остальных нервных тканей в центральной нервной системе. Это поможет исследователям лучше осознать нейродегенеративные заболевания, включая ослепляющие заболевания сетчатки, такие как возрастная макулярная дегенерация.
Не считая того, потенциальные способы исцеления могут быть протестированы на многофункциональных клеточках людского глаза, что дозволяет убыстрить разработку способов исцеления без использования лабораторных звериных. Франс Винберг отмечает, что таковой подход может понизить издержки на исследования по сопоставлению с работой на нечеловеческих приматах и опорой на модели звериных, получая результаты, которые не постоянно применимы к человеку. К примеру, хотя мыши обширно употребляются в исследовательских работах зрения, у их нет макулы, в отличие от нас.
С иной стороны, Энн Ханнекен гласит, что эти результаты точно посодействуют в производстве жизнестойких заплаток из тканей сетчатки человека для исцеления болезней, приводящих к слепоте. Она разъясняет: “До сего времени не удавалось вынудить клеточки всех разных слоев центральной сетчатки разговаривать вместе, как это обычно происходит в жив сетчатке. В дальнейшем мы сможем употреблять этот подход для разработки способов исцеления, направленных на улучшение зрения и световых сигналов в очах с макулярными болезнями, таковыми как возрастная макулярная дегенерация”.
В конце концов, данное исследование присоединяется к своду научных трудов, посвященных необратимой природе либо необратимости погибели. В 2018 году исследователям из Йельского института удалось “воскресить” мозг свиньи через 4 часа опосля ее погибели, не сумев, но, вернуть глобальную активность нейронов. Процедура проходила по той же схеме, т.е. восстановление кровообращения, обеспечивающее поступление нужного кислорода и питательных веществ. Данные, собранные Аббасом и др., могут отдать ценную информацию для будущих посмертных тестов.
Источник
Читайте далее: